Aminosyra
Från Rilpedia
| Denna artikel är en del i serien Ämnesomsättningen med följande delar: |
| Metabolism |
| Katabolism |
| Anabolism |
| Katabolism |
| Matspjälkning |
| Glykolys |
| Beta-oxidation |
| Trans-/Deaminering |
| Citronsyracykeln |
| Elektrontransportkedjan |
| Oxidativ fosforylering |
| Ureacykeln |
| Anabolism |
| Glukoneogenes |
| Proteinsyntes |
| Fettsyrasyntes |
| Se även |
| Fotosyntes |
| Cellandning |
En aminosyra är en kemisk förening som innehåller både en amingrupp och en karboxylgrupp. Inom biokemin syftar ordet oftast på de 20 aminosyror som proteiner vanligtvis består av (det finns undantag i vissa organismer), trots att aminosyran prolin rent kemiskt inte är en aminosyra (utan en iminosyra) och att även andra aminosyror har biologisk betydelse. Proteiner är polymerer av alfa-aminosyror, som hålls ihop av peptidbindningar mellan kolet i en karboxylgrupp och kvävet i amingruppen på nästa aminosyra. I alfa-aminosyrorna, som även utanför proteiner är de vanligaste aminosyrorna, är amingruppen bunden till den första kolatomen, alfa-kolet, efter karboxylgruppen. Alfa-kolet är också bundet till en väteatom och till en sidokedja, som är speciell för respektive aminosyra.
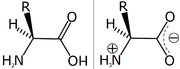
Aminosyror brukar vanligen delas in i grupper efter sidokedjornas egenskaper: sura, basiska, hydrofila (eller polära) och hydrofoba (eller opolära). Alla aminosyror är amfolyter, då den både kan ta upp och avge protoner. Karboxylgruppen kan avge en proton till amingruppen, då aminosyran bildar en amfojon, även kallat zwitterjon. Zwitterjonen är amfolyt och dipolär. Vid den isoelektriska punkten föreligger alltså nettoladdning noll.
Prolin har en lite annorlunda molekylstruktur än andra aminosyror. Den är stor, har starka kovalenta bindningar och en fyrkantig struktur som gör den väldigt styv.
Essentiella aminosyror är aminosyror som kroppen inte kan tillverka genom att bygga om andra aminosyror och som därför måste tillföras via kosten.
Omvandling av aminosyror
Alla aminosyror kan omvandlas till karboxylsyror genom att ta bort dess aminogrupp. Detta kan ske genom två olika metoder, transaminering och deaminering. Transaminering innebär att aminogruppen förs över från aminosyran till en karboxylsyra enligt formeln:
- aminosyra1 + karboxylsyra2
 karboxylsyra1 + aminosyra2
karboxylsyra1 + aminosyra2
Om det istället finns ett överskott av aminosyror så kan de deamineras, vilket innebär att aminosyran oxideras till en karboxylsyra och ammoniak som är mycket giftigt och omedelbart görs till urinämne.
Karboxylsyrorna som kommer från de- och transamineringen kan sedan antingen skapas om till aminosyror igen eller brytas ner. Flera kan ingå i citronsyracykeln medan andra får andra nedbrytningsvägar.
Indelning
Aminosyror delas in fyra eller fem grupper (beroende på skola) med avseende på sina sidokedjor. De fyra är:
- Ickepolära sidokedjor (hydrofob)
- Oladdade polära sidokedjor (hydrofil)
- Sura sidokedjor
- Basiska sidokedjor
De sura sidokedjorna (karboxyl-sura) är negativt laddade i neutrala miljöer.
En kemiskt användbar aminosyra är histidin som kan fås att byta laddning. Ett exempel på användningsområde är histidin-tagg vid rening av proteiner med hjälp av kolonn. Då kan man först hälla i sitt blandade startmaterial och få analyten att fästa till kolonnen (tex. positiv analyt binder till negativt histidin i kolonnen). Sedan byter man laddning på histidin som då vid sköljning av kolonnen släpper ifrån sig den isolerade substansen.
2 aminosyror bildar en dipeptid, 3 aminosyror bildar en tripeptid och så vidare. Mer än 10 aminosyror bildar en polypeptid, och mer än 50-100 aminosyror bildar ett protein. Aminosyror i en peptid eller ett protein kallas för aminosyrarest.
Kemiska egenskaper
Den här tabellen visar för varje aminosyra i proteiner:
- Vanligt förekommande en-bokstavs-förkortning
- Vanligt förekommande tre-bokstavs-förkortning
- Sidogruppens kemiska egenskaper
| Förkortn. | Fullständigt namn | Typ av sidogrupp | Massa | pI | pKa1 (α-COOH) | pKa2 (α-+NH3) | pKaR (R) | Kommentarer | |
|---|---|---|---|---|---|---|---|---|---|
| A | Ala | Alanin | hydrofob | 89,09 | 6,11 | 2,35 | 9,87 | ||
| C | Cys | Cystein | hydrofil | 121,16 | 5,05 | 1,92 | 10,70 | 8,37 | I oxiderande miljö kan två cysteiner binda kovalent till varandra, disulfidbindning. Denna bindning stabiliserar proteiners tertiärstruktur, till exempel i insulin. |
| D | Asp | Asparaginsyra | syra | 133,10 | 2,85 | 1,99 | 9,90 | 3,90 | |
| E | Glu | Glutaminsyra | syra | 147,13 | 3,15 | 2,10 | 9,47 | 4,07 | |
| F | Phe | Fenylalanin | hydrofob | 165,19 | 5,49 | 2,20 | 9,31 | ||
| G | Gly | Glycin | hydrofob | 75,07 | 6,06 | 2,35 | 9,78 | Eftersom α-kolet binder till två lika "grupper", väteatomer, är glycin inte optiskt aktivt. | |
| H | His | Histidin | basisk | 155,16 | 7,60 | 1,80 | 9,33 | 6,04 | |
| I | Ile | Isoleucin | hydrofob | 131,17 | 6,05 | 2,32 | 9,76 | ||
| K | Lys | Lysin | basisk | 146,19 | 9,60 | 2,16 | 9,06 | 10,54 | |
| L | Leu | Leucin | hydrofob | 131,17 | 6,01 | 2,33 | 9,74 | ||
| M | Met | Metionin | hydrofob | 149,21 | 5,74 | 2,13 | 9,28 | Syntesen (tillverkningen) av nya proteiner i cellerna börjar alltid med en metionin. I många fall tas denna bort i senare processer. | |
| N | Asn | Asparagin | hydrofil | 132,12 | 5,41 | 2,14 | 8,72 | ||
| P | Pro | Prolin | hydrofob | 115,13 | 6,30 | 1,95 | 10,64 | ||
| Q | Gln | Glutamin | hydrofil | 146,15 | 5,65 | 2,17 | 9,13 | ||
| R | Arg | Arginin | basisk | 174,20 | 10,76 | 1,82 | 8,99 | 12,48 | |
| S | Ser | Serin | hydrofil | 105,09 | 5,68 | 2,19 | 9,21 | ||
| T | Thr | Treonin | hydrofil | 119,12 | 5,60 | 2,09 | 9,10 | ||
| V | Val | Valin | hydrofob | 117,15 | 6,00 | 2,39 | 9,74 | ||
| W | Trp | Tryptofan | hydrofob | 204,23 | 5,89 | 2,46 | 9,41 | ||
| Y | Tyr | Tyrosin | hydrofil | 181,19 | 5,64 | 2,20 | 9,21 | 10,46 | |
|
|||||