Natriumhydroxid
Från Rilpedia
m (rubrikputs) |
RIL (Diskussion | bidrag) (Rev: 13 maj 2010 kl. 00.46 SieBot m (7 780 byte) (robot Lägger till: ms:Natrium hidroksida) (revid: http://sv.wikipedia.org/w/index.php?title=Natriumhydroxid&oldid=11692325)) |
||
| Rad 1: | Rad 1: | ||
<noinclude>{{rpsv.from.wpsv}}</noinclude> | <noinclude>{{rpsv.from.wpsv}}</noinclude> | ||
{{Kemibox | {{Kemibox | ||
| - | |Vardagligt namn = | + | |Vardagligt namn = Natriumhydroxid |
|Bild = Sodium hydroxide.jpg | |Bild = Sodium hydroxide.jpg | ||
|Bildtext = Natriumhydroxid | |Bildtext = Natriumhydroxid | ||
|Bildbredd = 200 | |Bildbredd = 200 | ||
| - | |Bild2 = | + | |Bild2 = |
| - | |Bild2text = | + | |Bild2text = |
| - | |Systematiskt namn = | + | |Systematiskt namn = Natriumhydroxid |
| - | |Övriga namn = | + | |Övriga namn = Natronlut |
| - | |Kemisk formel = [[ | + | |Kemisk formel = [[Natrium|Na]][[Hydroxid|OH]] |
|Utseende = Vit, fast | |Utseende = Vit, fast | ||
|CAS-nummer = 1310-73-2 | |CAS-nummer = 1310-73-2 | ||
| - | |SMILES = | + | |SMILES = [Na+].[OH-] |
|Molmassa = 40,0 | |Molmassa = 40,0 | ||
|Densitet = 2,1 | |Densitet = 2,1 | ||
| Rad 18: | Rad 18: | ||
|LöslighetTemp = 20 | |LöslighetTemp = 20 | ||
|Smältpunkt = 326 | |Smältpunkt = 326 | ||
| - | |Smältextra = | + | |Smältextra = |
|Kokpunkt = 1390 | |Kokpunkt = 1390 | ||
| - | |Huvudfara = | + | |Huvudfara = {{Farosymbol|C}} |
| - | |NFPA704 = | + | |NFPA704 = {{NFPA 704|Hälsa=3|Eldfarlighet=0|Reaktivitet=2}} |
|}} | |}} | ||
| - | |||
| - | Natriumhydroxid | + | '''Natriumhydroxid''', [[natrium|Na]][[hydroxidjon|OH]], är ett vitt, fast ämne som är en [[bas (kemi)|Arrheniusbas]], det vill säga ger ifrån sig hydroxidjoner (OH<sup>-</sup>) i [[vatten]]lösning. OH<sup>-</sup> är en stark [[bas (kemi)|Brønsted-Lowry-bas]], så vattenlösningar av natriumhydroxid, som kallas '''natronlut''' eller bara '''lut''', är starkt frätande. Natriumhydroxid är mycket lättlösligt i vatten. Det framställs genom [[elektrolys|elektrolytisk]] sönderdelning av [[natriumklorid]] i en delad cell. |
| - | ==Egenskaper== | + | Natriumhydroxid har många namn såsom kaustiksoda, kaustisk soda, kaustiskt natron, natron (vilket dock oftare används om [[natriumbikarbonat]]), natronhydrat, natriumhydrat, mineraliskt kali, alkali minerali eller etsnatron. |
| + | |||
| + | == Egenskaper == | ||
Natriumhydroxid löser sig fullständigt i vatten. Basen löser sig även i [[etanol]] och [[metanol]] men inte lika bra som [[kaliumhydroxid]]. Natriumhydroxid är olösligt i [[opolär]]a lösningsmedel som [[Eter (kemikalie)|eter]]. | Natriumhydroxid löser sig fullständigt i vatten. Basen löser sig även i [[etanol]] och [[metanol]] men inte lika bra som [[kaliumhydroxid]]. Natriumhydroxid är olösligt i [[opolär]]a lösningsmedel som [[Eter (kemikalie)|eter]]. | ||
| - | [[Kemisk bindning|Bindningen]] mellan natrium och hydroxid i föreningen är fullständigt [[jonbindning|jonisk]]. Hydroxidjonen gör natriumhydroxid till en stark bas som reagerar med [[syra|syror]] under bildning av vatten och ett korresponderande [[salter|salt]], till exempel vid reaktion med [[saltsyra]] bildas vatten och [[natriumklorid]]. | + | [[Kemisk bindning|Bindningen]] mellan natrium och hydroxid i föreningen är fullständigt [[jonbindning|jonisk]]. Hydroxidjonen gör natriumhydroxid till en stark bas som reagerar med [[syra|syror]] under bildning av vatten och ett korresponderande [[salter|salt]], till exempel vid reaktion med [[saltsyra]] bildas vatten och [[natriumklorid]]. |
:NaOH([[lösning (kemi)|aq]]) + [[Väteklorid|HCl]](aq) → [[natriumklorid|NaCl]](aq) + [[vatten|H<sub>2</sub>O]]([[vätska|l]]) | :NaOH([[lösning (kemi)|aq]]) + [[Väteklorid|HCl]](aq) → [[natriumklorid|NaCl]](aq) + [[vatten|H<sub>2</sub>O]]([[vätska|l]]) | ||
| Rad 36: | Rad 37: | ||
Oftast kan sådana [[neutralisering]]sreaktioner sammanfattas med en nettojonformel: | Oftast kan sådana [[neutralisering]]sreaktioner sammanfattas med en nettojonformel: | ||
| - | :[[Hydroxidjon|OH<sup> | + | :[[Hydroxidjon|OH<sup>−</sup>]](aq) + [[Hydroniumjon|H<sub>3</sub>O<sup>+</sup>(aq)]] → 2H<sub>2</sub>O |
Denna typ av reaktion, med en stark syra, genererar värme, och kallas därför en [[exoterm]] reaktion. Sådana syrabasreaktioner kan också användas för [[titrering]], en vanlig metod för att bestämma en syras [[koncentration]]. En annan typ av reaktion som natriumhydroxid kan vara inblandad i är med sura [[oxid]]er. Till exempel så absorberar basen [[koldioxid]] från luften och måste därför förvaras i ett lufttätt kärl. Natriumhydroxid reagerar också fullständigt med [[svaveldioxid]] (SO<sub>2</sub>), och kan användas för att "skrubba" (från engelskan ''scrub'', en process som avlägsnar en komponent i en gasblandning) bort giftiga sura gaser som SO<sub>2</sub> and [[Svavelväte|H<sub>2</sub>S]] så att de inte släpps ut i [[jordens atmosfär|atmosfären]]. | Denna typ av reaktion, med en stark syra, genererar värme, och kallas därför en [[exoterm]] reaktion. Sådana syrabasreaktioner kan också användas för [[titrering]], en vanlig metod för att bestämma en syras [[koncentration]]. En annan typ av reaktion som natriumhydroxid kan vara inblandad i är med sura [[oxid]]er. Till exempel så absorberar basen [[koldioxid]] från luften och måste därför förvaras i ett lufttätt kärl. Natriumhydroxid reagerar också fullständigt med [[svaveldioxid]] (SO<sub>2</sub>), och kan användas för att "skrubba" (från engelskan ''scrub'', en process som avlägsnar en komponent i en gasblandning) bort giftiga sura gaser som SO<sub>2</sub> and [[Svavelväte|H<sub>2</sub>S]] så att de inte släpps ut i [[jordens atmosfär|atmosfären]]. | ||
| Rad 42: | Rad 43: | ||
:2NaOH + [[koldioxid|CO<sub>2</sub>]] → [[natriumkarbonat|Na<sub>2</sub>CO<sub>3</sub>]] + H<sub>2</sub>O | :2NaOH + [[koldioxid|CO<sub>2</sub>]] → [[natriumkarbonat|Na<sub>2</sub>CO<sub>3</sub>]] + H<sub>2</sub>O | ||
| - | Natriumhydroxid reagerar långsamt med [[glas]] och bildar [[natriumsilikat]], vilket kan påverka till exempel laboratoriekärl av glas. Glaskärl tar skada av långvarig kontakt med natriumhydroxid. Natriumhydroxid angriper inte [[järn]] eller [[koppar]], men däremot andra [[metall]]er som [[aluminium]], [[zink]] och [[titan]]. Aluminium får därför aldrig tvättas med natriumhydroxid. | + | Natriumhydroxid reagerar långsamt med [[glas]] och bildar [[natriumsilikat]], vilket kan påverka till exempel laboratoriekärl av glas. Glaskärl tar skada av långvarig kontakt med natriumhydroxid. Natriumhydroxid angriper inte [[järn]] eller [[koppar]], men däremot andra [[metall]]er som [[aluminium]], [[zink]] och [[Titan (grundämne)|titan]]. Aluminium får därför aldrig tvättas med natriumhydroxid. |
:2[[Aluminium|Al]]([[fast|s]]) + 6NaOH(aq) → 3[[väte|H<sub>2</sub>]]([[Gas|g]]) + 2Na<sub>3</sub>AlO<sub>3</sub>(aq) | :2[[Aluminium|Al]]([[fast|s]]) + 6NaOH(aq) → 3[[väte|H<sub>2</sub>]]([[Gas|g]]) + 2Na<sub>3</sub>AlO<sub>3</sub>(aq) | ||
| - | Många icke-metaller reagerar också med natriumhydroxid under bildning av salter. Till exempel bildar [[fosfor]] [[natriumhypofosfit]], medan [[kisel]] ger [[natriumsilikat]]. | + | Många icke-metaller reagerar också med natriumhydroxid under bildning av salter. Till exempel bildar [[fosfor]] [[natriumhypofosfit]], medan [[kisel]] ger [[natriumsilikat]]. |
| - | Till skillnad från natriumhydroxid är de flesta metallers hydroxider olösliga i vatten, varför natirumhydroxid kan användas för att fälla ut metallhydroxider. En sådan metallhydroxid är [[aluminiumhydroxid]] som används som [[aggregering|flockningsmedel]] för att filtrera bort partiklar vid [[vattenrening]]. Aluminiumhydroxid framställs vid reningsanläggningen från [[aluminiumsulfat]] genom att | + | Till skillnad från natriumhydroxid är de flesta metallers hydroxider olösliga i vatten, varför natirumhydroxid kan användas för att fälla ut metallhydroxider. En sådan metallhydroxid är [[aluminiumhydroxid]] som används som [[aggregering|flockningsmedel]] för att filtrera bort partiklar vid [[vattenrening]]. Aluminiumhydroxid framställs vid reningsanläggningen från [[aluminiumsulfat]] genom att låta det reagera med natriumhydroxid NaOH: |
:6NaOH(aq) + [[Aluminiumsulfat|Al<sub>2</sub>(SO<sub>4</sub>)<sub>3</sub>]](aq) → 2[[Aluminiumhydroxid|Al(OH)<sub>3</sub>]](s) + 3[[natriumsulfat|Na<sub>2</sub>SO<sub>4</sub>]](aq) | :6NaOH(aq) + [[Aluminiumsulfat|Al<sub>2</sub>(SO<sub>4</sub>)<sub>3</sub>]](aq) → 2[[Aluminiumhydroxid|Al(OH)<sub>3</sub>]](s) + 3[[natriumsulfat|Na<sub>2</sub>SO<sub>4</sub>]](aq) | ||
| Rad 56: | Rad 57: | ||
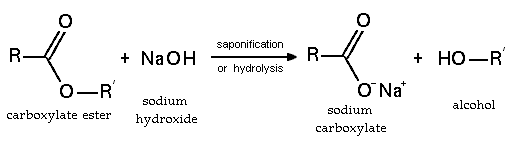
[[Fil:Ester hydrolysis.png|frame|center|Basisk hydrolys av en ester]] | [[Fil:Ester hydrolysis.png|frame|center|Basisk hydrolys av en ester]] | ||
| - | ==Användning== | + | == Användning == |
Natriumhydroxid används som stark bas vid tillverkning av många kemikalier och andra produkter, såsom [[pappersmassa]], [[textil]]er, [[dricksvatten]], [[tvål]] och [[tvättmedel]]. Natriumhydroxid används även som [[propplösare]]. Speciellt inom [[massa- och pappersindustri]]n används enorma mängder natriumhydroxid. Vid massafabriker som utnyttjar [[sulfatprocessen]] både förbrukas och genereras stora mängder kontinuerligt - basen används för att lösa upp [[lignin]]et i [[ved]], förbränns tillsammans med det utlösta materialet i en [[sodapanna]] och återskapas sedan i en så kallad kaustiseringsanläggning. | Natriumhydroxid används som stark bas vid tillverkning av många kemikalier och andra produkter, såsom [[pappersmassa]], [[textil]]er, [[dricksvatten]], [[tvål]] och [[tvättmedel]]. Natriumhydroxid används även som [[propplösare]]. Speciellt inom [[massa- och pappersindustri]]n används enorma mängder natriumhydroxid. Vid massafabriker som utnyttjar [[sulfatprocessen]] både förbrukas och genereras stora mängder kontinuerligt - basen används för att lösa upp [[lignin]]et i [[ved]], förbränns tillsammans med det utlösta materialet i en [[sodapanna]] och återskapas sedan i en så kallad kaustiseringsanläggning. | ||
I [[matlagning]] används natriumhydroxid till till exempel [[lutfisk]] och blötläggning av [[oliv]]er. Som [[livsmedelstillsats]] har det [[E-nummer]] E 524. Natriumhydroxid förekommer också vid framställning av [[tvål]]produkter. Om man får vattenlösning av natriumhydroxid på händerna känns det som tvålvatten, lösningen förvandlar nämligen hudens eget fett till tvål. Detta bör man inte testa då det är mycket skadligt för huden. | I [[matlagning]] används natriumhydroxid till till exempel [[lutfisk]] och blötläggning av [[oliv]]er. Som [[livsmedelstillsats]] har det [[E-nummer]] E 524. Natriumhydroxid förekommer också vid framställning av [[tvål]]produkter. Om man får vattenlösning av natriumhydroxid på händerna känns det som tvålvatten, lösningen förvandlar nämligen hudens eget fett till tvål. Detta bör man inte testa då det är mycket skadligt för huden. | ||
| - | ==Källor== | + | == Källor == |
| - | *{{översatt|url=http://en.wikipedia.org/w/index.php?title=Sodium_hydroxide&oldid=179149561|språkversion=engelskspråkiga}} | + | * {{översatt|url=http://en.wikipedia.org/w/index.php?title=Sodium_hydroxide&oldid=179149561|språkversion=engelskspråkiga}} |
| + | |||
| + | == Se även == | ||
| + | * [[Kaliumhydroxid]] | ||
[[Kategori:Surhetsreglerande medel]] | [[Kategori:Surhetsreglerande medel]] | ||
| Rad 76: | Rad 80: | ||
[[da:Natriumhydroxid]] | [[da:Natriumhydroxid]] | ||
[[de:Natriumhydroxid]] | [[de:Natriumhydroxid]] | ||
| + | [[el:Υδροξείδιο του νατρίου]] | ||
[[en:Sodium hydroxide]] | [[en:Sodium hydroxide]] | ||
[[es:Hidróxido de sodio]] | [[es:Hidróxido de sodio]] | ||
[[et:Naatriumhüdroksiid]] | [[et:Naatriumhüdroksiid]] | ||
| + | [[fa:سدیم هیدروکسید]] | ||
[[fi:Natriumhydroksidi]] | [[fi:Natriumhydroksidi]] | ||
[[fr:Hydroxyde de sodium]] | [[fr:Hydroxyde de sodium]] | ||
| Rad 84: | Rad 90: | ||
[[he:נתרן הידרוקסידי]] | [[he:נתרן הידרוקסידי]] | ||
[[hu:Nátrium-hidroxid]] | [[hu:Nátrium-hidroxid]] | ||
| + | [[hy:Նատրիումի հիդրօքսիդ]] | ||
[[id:Natrium hidroksida]] | [[id:Natrium hidroksida]] | ||
[[is:Vítissódi]] | [[is:Vítissódi]] | ||
[[it:Idrossido di sodio]] | [[it:Idrossido di sodio]] | ||
[[ja:水酸化ナトリウム]] | [[ja:水酸化ナトリウム]] | ||
| + | [[ka:ნატრიუმის ჰიდროქსიდი]] | ||
[[ko:수산화 나트륨]] | [[ko:수산화 나트륨]] | ||
[[la:Lixivium]] | [[la:Lixivium]] | ||
| Rad 94: | Rad 102: | ||
[[mk:Натриум хидроксид]] | [[mk:Натриум хидроксид]] | ||
[[ml:സോഡിയം ഹൈഡ്രോക്സൈഡ്]] | [[ml:സോഡിയം ഹൈഡ്രോക്സൈഡ്]] | ||
| + | [[ms:Natrium hidroksida]] | ||
[[nds:Natriumhydroxid]] | [[nds:Natriumhydroxid]] | ||
[[nl:Natriumhydroxide]] | [[nl:Natriumhydroxide]] | ||
Nuvarande version från 29 maj 2010 kl. 18.55
| Natriumhydroxid | |
|---|---|
 |
|
| Systematiskt namn | Natriumhydroxid |
| Övriga namn | Natronlut |
| Kemisk formel | NaOH |
| Molmassa | 40,0 g/mol |
| Utseende | Vit, fast |
| CAS-nummer | 1310-73-2 |
| SMILES | [Na+].[OH-] |
| Egenskaper | |
| Densitet | 2,1 g/cm³ |
| Löslighet (vatten) | 1110 g/l (20 °C) |
| Smältpunkt | 326 °C |
| Kokpunkt | 1390 °C |
| Faror | |
| Huvudfara | |
| NFPA 704 | |
| SI-enheter & STP används om ej annat angivits | |
Natriumhydroxid, NaOH, är ett vitt, fast ämne som är en Arrheniusbas, det vill säga ger ifrån sig hydroxidjoner (OH-) i vattenlösning. OH- är en stark Brønsted-Lowry-bas, så vattenlösningar av natriumhydroxid, som kallas natronlut eller bara lut, är starkt frätande. Natriumhydroxid är mycket lättlösligt i vatten. Det framställs genom elektrolytisk sönderdelning av natriumklorid i en delad cell.
Natriumhydroxid har många namn såsom kaustiksoda, kaustisk soda, kaustiskt natron, natron (vilket dock oftare används om natriumbikarbonat), natronhydrat, natriumhydrat, mineraliskt kali, alkali minerali eller etsnatron.
Innehåll |
Egenskaper
Natriumhydroxid löser sig fullständigt i vatten. Basen löser sig även i etanol och metanol men inte lika bra som kaliumhydroxid. Natriumhydroxid är olösligt i opolära lösningsmedel som eter.
Bindningen mellan natrium och hydroxid i föreningen är fullständigt jonisk. Hydroxidjonen gör natriumhydroxid till en stark bas som reagerar med syror under bildning av vatten och ett korresponderande salt, till exempel vid reaktion med saltsyra bildas vatten och natriumklorid.
Oftast kan sådana neutraliseringsreaktioner sammanfattas med en nettojonformel:
Denna typ av reaktion, med en stark syra, genererar värme, och kallas därför en exoterm reaktion. Sådana syrabasreaktioner kan också användas för titrering, en vanlig metod för att bestämma en syras koncentration. En annan typ av reaktion som natriumhydroxid kan vara inblandad i är med sura oxider. Till exempel så absorberar basen koldioxid från luften och måste därför förvaras i ett lufttätt kärl. Natriumhydroxid reagerar också fullständigt med svaveldioxid (SO2), och kan användas för att "skrubba" (från engelskan scrub, en process som avlägsnar en komponent i en gasblandning) bort giftiga sura gaser som SO2 and H2S så att de inte släpps ut i atmosfären.
Natriumhydroxid reagerar långsamt med glas och bildar natriumsilikat, vilket kan påverka till exempel laboratoriekärl av glas. Glaskärl tar skada av långvarig kontakt med natriumhydroxid. Natriumhydroxid angriper inte järn eller koppar, men däremot andra metaller som aluminium, zink och titan. Aluminium får därför aldrig tvättas med natriumhydroxid.
Många icke-metaller reagerar också med natriumhydroxid under bildning av salter. Till exempel bildar fosfor natriumhypofosfit, medan kisel ger natriumsilikat.
Till skillnad från natriumhydroxid är de flesta metallers hydroxider olösliga i vatten, varför natirumhydroxid kan användas för att fälla ut metallhydroxider. En sådan metallhydroxid är aluminiumhydroxid som används som flockningsmedel för att filtrera bort partiklar vid vattenrening. Aluminiumhydroxid framställs vid reningsanläggningen från aluminiumsulfat genom att låta det reagera med natriumhydroxid NaOH:
Natriumhydroxid reagerar även med karboxylsyror under bildning av deras salter och är till och med tillräckligt starkt för att bilda salter med fenoler. Natriumhydroxid kan användas för basdriven hydrolys av estrar (såsom vid förtvålning), amider och alkylhalider.
Användning
Natriumhydroxid används som stark bas vid tillverkning av många kemikalier och andra produkter, såsom pappersmassa, textiler, dricksvatten, tvål och tvättmedel. Natriumhydroxid används även som propplösare. Speciellt inom massa- och pappersindustrin används enorma mängder natriumhydroxid. Vid massafabriker som utnyttjar sulfatprocessen både förbrukas och genereras stora mängder kontinuerligt - basen används för att lösa upp ligninet i ved, förbränns tillsammans med det utlösta materialet i en sodapanna och återskapas sedan i en så kallad kaustiseringsanläggning.
I matlagning används natriumhydroxid till till exempel lutfisk och blötläggning av oliver. Som livsmedelstillsats har det E-nummer E 524. Natriumhydroxid förekommer också vid framställning av tvålprodukter. Om man får vattenlösning av natriumhydroxid på händerna känns det som tvålvatten, lösningen förvandlar nämligen hudens eget fett till tvål. Detta bör man inte testa då det är mycket skadligt för huden.
Källor
- Artikeln är, helt eller delvis, en översättning från engelskspråkiga Wikipedia.