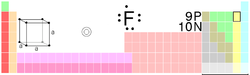
Fluor
Från Rilpedia
|
|||||||||||||||||||
| Allmänt | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Namn, kemiskt tecken, nummer | fluor, F, 9 | ||||||||||||||||||
| Ämnesklass | halogen | ||||||||||||||||||
| Grupp, period, block | 17, 2, p | ||||||||||||||||||
| Densitet | 1,696 kg/m3 (273 K) | ||||||||||||||||||
| Hårdhet | - | ||||||||||||||||||
| Utseende | blekt gul gas |
||||||||||||||||||
| Atomens egenskaper | |||||||||||||||||||
| Atommassa | 18,998403 u | ||||||||||||||||||
| Atomradie (beräknad) | 50 (42) pm | ||||||||||||||||||
| Kovalent radie | 71 pm | ||||||||||||||||||
| van der Waalsradie | 147 pm | ||||||||||||||||||
| Elektronkonfiguration | [ He ]2s22p5 | ||||||||||||||||||
| e− per skal | 2,7 | ||||||||||||||||||
| Oxidationstillstånd (oxid) | −1 (starkt sur) | ||||||||||||||||||
| Kristallstruktur | kubisk | ||||||||||||||||||
| Ämnets fysiska egenskaper | |||||||||||||||||||
| Aggregationstillstånd | gas | ||||||||||||||||||
| Magnetiska egenskaper | icke magnetisk | ||||||||||||||||||
| Smältpunkt | 53,53 K (−220 °C) | ||||||||||||||||||
| Kokpunkt | 85,03 K (−188 °C) | ||||||||||||||||||
| Molvolym | 11,2 ·10- m3/mol | ||||||||||||||||||
| Ångbildningsvärme | 3,2698 kJ/mol | ||||||||||||||||||
| Smältvärme | 0,2552 kJ/mol | ||||||||||||||||||
| Ångtryck | - | ||||||||||||||||||
| Ljudhastighet | - m/s vid 293,15 K | ||||||||||||||||||
| Diverse | |||||||||||||||||||
| Elektronegativitet | 3,98 (Paulingskalan) | ||||||||||||||||||
| Värmekapacitet | 824 J/(kg·K) | ||||||||||||||||||
| Elektrisk ledningsförmåga | ___ ·106 S/m (Ω−1·m−1) | ||||||||||||||||||
| Värmeledningsförmåga | 0,0279 W/(m·K) | ||||||||||||||||||
| 1a jonisationspotential | 1681 kJ/mol | ||||||||||||||||||
| 2a jonisationspotential | 3374,2 kJ/mol | ||||||||||||||||||
| 3e jonisationspotential | 6050,4 kJ/mol | ||||||||||||||||||
| 4e jonisationspotential | 8407,7 kJ/mol | ||||||||||||||||||
| 5e jonisationspotential | 11022,7 kJ/mol | ||||||||||||||||||
| 6e jonisationspotential | 15164,1 kJ/mol | ||||||||||||||||||
| 7e jonisationspotential | 17868 kJ/mol | ||||||||||||||||||
| 8e jonisationspotential | 92038,1 kJ/mol | ||||||||||||||||||
| 9e jonisationspotential | 106434,3 kJ/mol | ||||||||||||||||||
| Mest stabila isotoper | |||||||||||||||||||
|
|||||||||||||||||||
| SI-enheter & STP används om ej annat angivits | |||||||||||||||||||
Fluor är ett icke-metalliskt grundämne med atomnummer 9 och kemiskt tecken F, tillhörande gruppen halogener. Fluor är en mycket giftig, blekt gul gas bestående av molekyler (F2). Fluor är det mest reaktiva och elektronegativa av alla grundämnen, och reagerar med alla övriga grundämnen utom de två lättaste ädelgaserna helium och neon. Även vatten brinner med ljus låga i fluoratmosfär. Fluor förekommer därför inte i ren form i naturen.
Innehåll |
Historia
År 1670 upptäcktes att glas kunde etsas av en blandning av flusspat (kalciumfluorid) och svavelsyra. Snart förstod man att den syra som bildades innehöll ett okänt grundämne. Nästa problem var att isolera grundämnet. Först år 1886 lyckades detta av Henri Moissan, genom elektrolys av kaliumvätefluorid löst i vattenfri vätefluorid i vätskeform vid −50 °C. Moissan fick 1906 nobelpriset i kemi för sina arbeten med fluor.
Framställning
Fluor framställs industriellt med en metod som i stort sett är Moissans ursprungliga, se ovan.
Användningsområden
Fluor förekommer i föreningar som bland annat används för att skydda mot karies, till exempel natriumfluorid (NaF), en aktiv komponent i fluorsköljningar och tandkräm.
Se även