Ättiksyra
Från Rilpedia
| Ättiksyra | |
|---|---|
Ättiksyra 2-D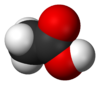 |
|
| Systematiskt namn | Etansyra |
| Kemisk formel | C2H4O2 CH3COOH |
| Molmassa | 60,05 g/mol |
| Utseende | Färglös, vätska |
| CAS-nummer | 64-19-7 |
| SMILES | CC(=O)O |
| Egenskaper | |
| Densitet | 1,049 g/cm³ |
| Löslighet (vatten) | Löslig |
| Smältpunkt | 16,7 °C |
| Kokpunkt | 118,1 °C |
| Faror | |
| Huvudfara | Frätande |
| NFPA 704 | |
| SI-enheter & STP används om ej annat angivits | |
Ättiksyra, CH3COOH, (systematiskt namn etansyra) är den enklaste karboxylsyran näst myrsyra. Den är, i 12-procentig (ättiksprit) eller 24-procentig (ättika) lösning, vanligt förekommande i hushållen, och används för konservering av olika sorters matvaror. Ättiksyra har smältpunkt cirka 16 °C vilket har gett den rena syran namnet isättika eftersom den liknar is under smältpunkten. Dess relativt höga smältpunkt och kokpunkt 118 °C kan förklaras genom att den bildar vätebundna dimerer. Ättiksyras pKa är 4,79. Syran bildar lätt salter som kallas acetater som precis som nitrater är lösliga i vatten. I innehållsförteckningar på livsmedel används E-nummer E 260 för ättiksyra. Årligen används cirka 6,5 miljoner ton ättiksyra, varav en mindre del är återvunnen.
Innehåll |
Medicin
Kroppen bryter ner etanol till ättiksyra vilket är ett för kroppen naturligt ämne.
Användning
En stor del av ättiksyran som produceras används till framställning av vinylacetat som används till polymer, och estrar som etylacetat som används som lösningsmedel i målarfärger. Ättiksyra används också för tillverkning av ättiksyraanhydrid som sedan kan användas till tillverkning av cellulosaacetat (som används till tyg, film med mera) och acetylsalicylsyra (Som bland annat ingår i t.ex aspirin). Ättiksyraanhydrid bildar med morfin drogen heroin, ett starkt narkotikum.
Många estrar produceras genom reaktion mellan en alkohol och ättiksyra, dessa estrar kallas acetater som till exempel metylacetat, etylacetat, butylacetat, propylacetat och amylacetat. Andra användningsområden för ättiksyra är:
- Plaster
- Lim
- Färg
- Olika lösningsmedel
- Läkemedel
Säkerhet
Även om ättiksyra är en organisk syra kan den i höga koncentrationer vara frätande. Koncentrerad ättiksyra kan också vid höga temperaturer brinna.
| Koncentration | Märksymbol |
|---|---|
| 10 %-25 % | Irriterande (Xi) |
| 25 %-90 % | Frätande (C) |
| >90 % | Frätande (C) |
Lösningar med högre koncentrationer än 25 % kan ge ifrån sig frätande ångor, men lägre koncentrationer som 5 % är ganska ofarliga förutom om man dricker lösningen, då strupen kan skadas.
Se även






