Salpetersyra
Från Rilpedia
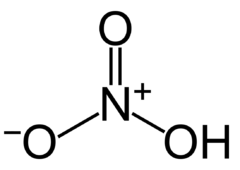
Salpetersyra (av latinets sal, salt och peter, klippa, se salpeter) är en starkt frätande syra med kemisk beteckning HNO3. Har en stickande lukt. Den protolyseras fullständigt i vatten och har ett pKa på -2. Den framställs genom att lösa dikvävepentoxid, N2O5, i vatten.
Formel: N2O5 + H2O -> 2HNO3
Koncentrerad salpetersyra ryker vid rumstemperatur då nitrösa gaser (kväveoxider), i synnerhet NO2, avgår. Dessa ångor kan vara gul- eller rödaktiga, och är synnerligen irriterande, då de är giftiga och löser sig i fukt till att bilda små droppar av salpetersyra.
Syran används som reagent i laboratorier och ingrediens i både sprängämnen (nitroglycerin och TNT) och konstgödsel (ammoniumnitrat). Tillsammans med saltsyra bildar det kungsvatten, aqua regia, som är ett av mycket få ämnen som kan lösa guld och platina. De gamla bergsmännen kallade salpetersyran skedvatten (av tyska ordet scheiden, skilja, särskilja) eftersom det i malm kunde skilja silver från guld. Skedvattnet löser nämligen silver, men inte guld.
Salterna kallas nitrater, och är i allmänhet mycket lättlösliga i vatten.
Salpetersyra kan även bildas vid förbränning av fossila bränslen. Den vanligen stabila kvävgasen kan oxideras av luftens syre på grund av den höga temperaturen. En blandning av kväveoxider med olika oxidationstal (NOx) bildas. Dessa reagerar sedan med vattenånga i luften och bildar HNO3, vilket bidrar till försurningen av sjöar och vattendrag.