Nitroniumjon
Från Rilpedia
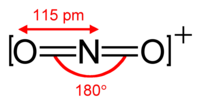
Nitroniumjonens bindningsavstånd och bindingsvinkel.
Nitroniumjon eller nitrylkatjon, NO2+, är inom kemin en i normala omständigheter ganska instabil jon som används vid nitreringar. På grund av dess instabilitet framställs det in situ genom att blanda koncentrerad svavelsyra med koncentrerad salpetersyra enligt reaktionerna:
- H2SO4 + HNO3 ↔ HSO4- + H2O+-NO2
-
- H2O+-NO2 ↔ NO2+ + H2O
Vattnet som frigörs protoneras omgående så jämvikten är starkt förskjuten åt höger. Vid närvaro av mer vatten minskar koncentrationen av nitroniumjoner och blandningens nitreringsförmåga minskar.
Nitroniumjonen NO2+ skall inte förväxlas med nitritjonen NO2−.
Litteratur
- Hägg, Gunnar, Allmän och oorganisk kemi (1966), Almquvist & Wiksell



