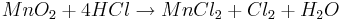Mangandioxid
Från Rilpedia
| Mangandioxid | |
|---|---|
_oxide.jpg/200px-Manganese(IV)_oxide.jpg) |
|
| Systematiskt namn | Mangandioxid |
| Övriga namn | Brunsten |
| Kemisk formel | MnO2 |
| Molmassa | 86,94 g/mol |
| Utseende | Svartbrun, pulver |
| CAS-nummer | 1313-13-9 |
| Egenskaper | |
| Densitet | 5,026 g/cm³ |
| Löslighet (vatten) | Olöslig |
| Smältpunkt | 535 °C (sönderdelas) |
| SI-enheter & STP används om ej annat angivits | |
Mangandioxid, MnO2, är en svartbrun oxid av mangan som finns naturligt i vissa malmer. Mangandioxid reagerar även med en smält alkaliemetallhydroxid och ett oxiderande ämne för att bilda en manganat.
Teknisk benämning på mangandioxid är brunsten.
Användning
Mangandioxid används i (brunstens-)batterier av zink-grafit-typen. I batteriet fungerar mangandioxiden som en elektrolyt. Saltet är även en katalysator för att få väteperoxid att sönderdela sig till vatten och syre, denna reaktion kan ge så mycket värme att vattnet börjar koka. Klor upptäcktes av Carl Wilhelm Scheele genom att låta saltsyra reagera med mangandioxid enligt följande reaktion.