Sulfoxid
Från Rilpedia
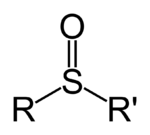
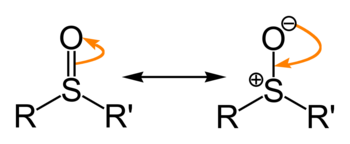
Sulfoxider är organiska föreningar innehållande sulfinylgruppen R-S(=O)-R’, där R och R’ är alkyl- eller arylgrupper. Sulfoxider kan ses som oxiderade sulfider, ur vilka de kan framställas genom oxidation med t.ex. en ekvivalent MCPBA. Omvänt kan de reduceras tillbaka till motsvarande sulfid med exempelvis litiumaluminiumhydrid. Bindningen stabiliseras genom resonans och ger upphov till ett stort dipolmoment, med den positiva laddningen förlagd till svavel och den negativa till syre.
Sulfoxider är trigonala pyramidala föreningar. Det fria elektronparets energibarriär för inversion är dock så pass hög (35-45 kcal/mol) att kirala föreningar är stabila vid rumstemperatur[1]. Flera läkemedel med kirala sulfoxider finns på marknaden t.ex. esomeprozol (Nexium).
Den enklaste sulfoxiden är DMSO, den är ett mycket bra lösningsmedel. Sulfoxider har sura α-väten, DMSO har pKa 35,1[2].
Källor
- ↑ Carey, Francis A., Sundberg, Richard J. Advanced Organic Chemistry, Part A: Structure and Mechanisms, 2000, 4th ed. ISBN 978-0-306-46243-6
- ↑ Acc. Chem. Res. 1988, 21, 456