ReO3-struktur
Från Rilpedia
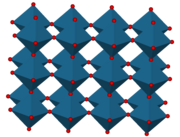
ReO3-strukturtypen är en kubisk strukturtyp som tillhör rymdgruppen Pm3m. Strukturtypen sammanfattar alla strukturer med stökiometrin AX3 där katjoner A och anjoner X sitter på samma sätt som i rhenium(VI)oxid (rheniumtrioxid, ReO3).
Strukturer med samma uppbyggnad men där A är anjonen och X katjonen sägs i stället vara av 'anti-ReO3-strukturtyp'.
Innehåll |
Egenskaper till föjd av strukturen, koordinationsgeometri
Varje katjon omges av sex anjoner i oktaedrisk koordination medan varje anjon omges av två katjoner i linjär koordination. I strukturen finns tomrum: stora dodekaedriska hål.
Föreningar som kristalliserar med ReO3-struktur
Rheniumtrioxid (ReO3), urantrioxid (UO3), molybdentrifluorid (MoF3), niobtrifluorid (NbF3), tantaltrifluorid (TaF3).
Föreningar som kristalliserar med anti-ReO3-struktur
Kopparnitrid (Cu3N).
Beskrivningar av ReO3-strukturen
Enhetscellen: katjonerna A sitter i cellens hörn och anjonerna X i mitten på cellkanterna, mellan två katjoner. Med sex kanter per hörn ger detta koordinationstal 6 för katjonen, medan anjonen har koordinationstal 2.
Polyedrar: strukturen byggs upp av AX6-oktaedrar som var och en delar alla sex oktaederhörn med en angränsande oktaeder per hörn.
Från tätpackning: kubisk tätpackning av anjoner X med 1/4 av anjonerna bortplockade i varje tätpackningsplan. I de oktaedriska hål som återstår efter utelämnande av 1/4 av anjonerna sitter katjoner. (De dodekaedriska hål som uppstår med koordinationstal 12 är dock för stora för katjonerna.)
Struktursläktskap:
- Rheniumtrioxidstrukturen motsvarar BX3-ramverket i perovskitstrukturen i perovskitstrukturen ABX3.
- AlF3-strukturen kan fås genom distorsion av ReO3-strukturen.
Radiekvoter: för katjon-anjonkontakt och inget anjon-anjonöverlapp krävs att katjonens radie r+ och anjonens radie r- förhåller sig som: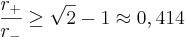
Källor
- West, Andrew: Basic Solid State Chemistry, 2nd ed., John Wiley & Sons, Inc, 1999. ISBN 0-471-987565-5.
- Müller, Ulrich: Anorganische Strukturchemie, Teubner men finns även översatt (&dyrare) hos John Wiley & Sons, Inc, 2004. ISBN 3-519-33512-3.
Externa länkar
 Wikimedia Commons har media som rör ReO3-struktur
Wikimedia Commons har media som rör ReO3-struktur