Autoprotolys
Från Rilpedia
Inom kemin är autoprotolys egenskapen hos ett rent amfolytiskt ämne att till viss del protolyseras, trots att ingen annan bas är närvarande. Detta innebär att en viss del av molekylerna kommer befinna sig i jonform.
Ett viktigt exempel är rent vatten, där vid rumstemperatur ungefär 1 molekyl på 560.000.000 protolyseras:
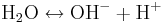
Vätejonen reagerar snabbt med en ny vattenmolekyl:
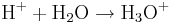
Detta innebär att även helt rent vatten innehåller en viss del oxoniumjoner (H3O+). Detta är även förklaringen till varför pH-skalan har sin neutrala punkt vid ungefär pH 7 (=-log (1/10.000.000)).
Se i övrigt under vattnets autoprotolys.



